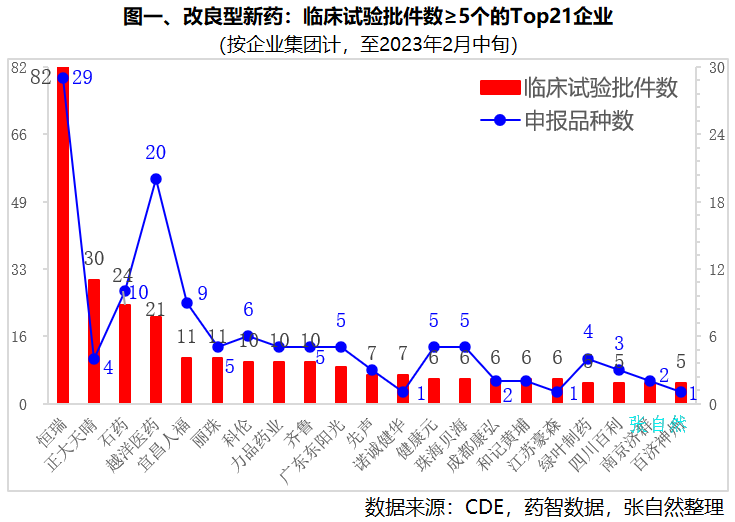
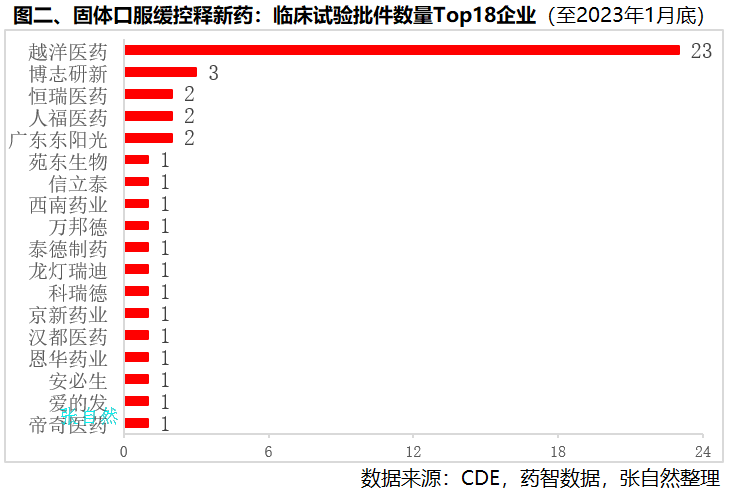
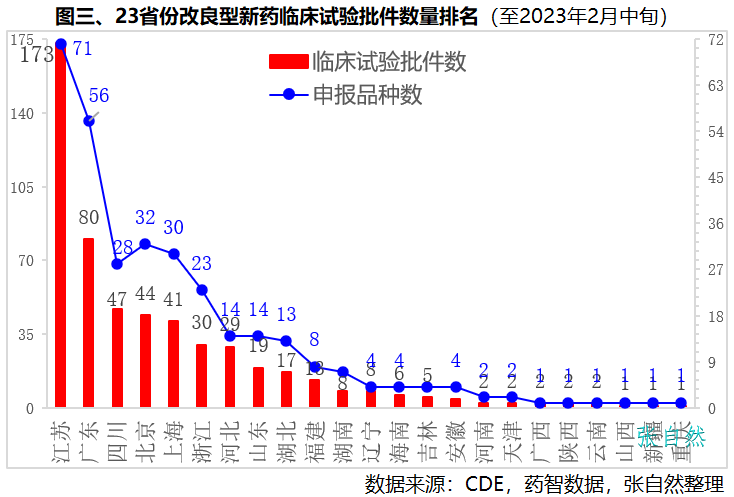
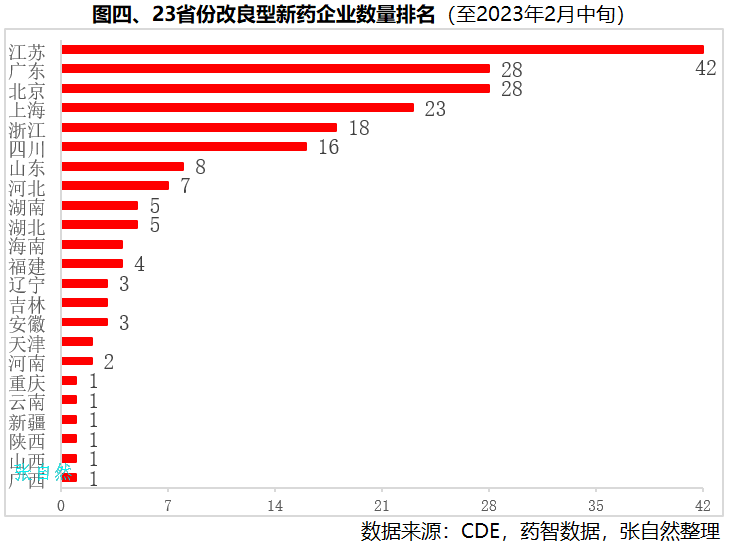
根据2016年CFDA发布的《化学药品注册分类改革工作方案》定义,改良型新药(即二类新药),是指在已知活性成分API的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,具有明显临床优势的药品。在仿制药面临集采竞价和新药研发难度不断加大的背景下,改良型新药因较创新药成功率高、耗资少、耗时短和较仿制药有一定的市场独占期等优势而日益受到重视。接作者已发表的《改良型新药开发进展|4图探秘》一文,本文再将我国改良型新药临床试验批件和研发企业的区域分布布做一汇总分析。截止今年2月中旬,全国共批准改良型新药临床试验537个,涉及322个品种。其中,江苏恒瑞获批临床试验最多,82个,占了全国的近六分之一(15.3%)。正大天晴(30个)、石药集团(24个)和越洋医药(21个)都超过20个,位居第2~4位。宜昌人福、丽珠集团都获批11个,并列第5。科伦、力品药业和齐鲁制药并列第6,都有10个临床试验批件。改良型新药临床试验涉及品种数最多的是恒瑞(29个品种)和越洋医药(20个品种),都涉及20个及以上品种。注:上述统计按企业集团计,如江苏恒瑞还包括旗下的上海恒瑞、成都盛迪、山东盛迪和福建盛迪医药。石药集团包括旗下石药中奇、中诺、欧意和恩必普药业等。(详见图一)截止今年1月底,全国共批准固体口服缓控释新药临床试验45个,其中越洋医药一家独大,获批23个,比全国其他所有企业之和还要多。越洋医药由国家级特聘专家(创业类)闻晓光博士创办,是中国化学制药工业协会改良型新药专业委员会主任委员单位,是应用自主创新和通用缓控释平台技术,开发适应美国(NDA/505(b)(2))、中国(化药2类)及全球市场新药的企业。其左乙拉西坦缓释片已由美国FDA批准上市、左乙拉西坦缓释片已申请中国上市受理、拉莫三嗪缓释片已申请美国上市受理。(详见图二)截止今年2月中旬,全国共批准改良型新药临床试验537个,除西部6省份(内蒙古、甘肃、宁夏、青海、西藏、贵州)以及黑龙江、江西外,全国23个省份都已有改良型新药临床试验获批。其中,江苏省最多,有173个,占了全国的三分之一(32.2%),比其后的广东(80个)、四川(47个)和北京(44)三省份总和还多。上海(41个)、浙江(30个)、河北(29个)和山东(19个)和湖北(17个)都获批15个以上临床试验。改良型新药临床试验涉及的品种数量,江苏也是最多的,共涉及71个品种。其次是广东(56个)、北京(32个)、上海(30个)和四川(28个)。(详见图三)截止今年2月中旬,全国批准的537个改良型新药临床试验分布在207家企业(按企业法人计,未归并到集团)。其中,江苏省的改良型新药企业最多,有42家,占了全国的五分之一,如恒瑞、正大天晴、越洋医药(泰州)、先声、豪森和南京济群等。广东和北京并列第二,都有28家企业,如广东的越洋医药(广州)、丽珠集团、广东东阳光和北京的诺诚健华、北京泰德制药等。上海有23家,上述四省份占了全国改良型新药研发企业总数的近六成(59.5%)。另外,浙江(18家)、四川(16家)、山东(8家)和河北(7家)也都有7家以上改良型新药研发企业。(详见图四)改良型新药作为我国传统制药企业转型升级的重要途径之一,研发格局初显,即将为改善广大患者的用药可及性贡献力量。